- فروش مواد شیمیایی
- مواد اولیه صنایع غذایی
- فروش ظروف آزمایشگاهی
- فروش تجهیزات
- مطالب مفید
- آگهی رایگان
- پیشنهادهای ویژه
- آموزش کار با سایت
- ورود به حساب کاربری
هیدروکلریک اسید یک اسید بسیار قوی با فرمول شیمیایی HCl و جرم مولی 36.46g/mol است. این اسید بی رنگ است ولی بوی بسیار تندی دارد. هیدروکلریک اسید با نام های دیگری مانند هیدروژن کلراید، تیرک، جوهر نمک، اسید کلروهیدریک نیز شناخته میشود. هیدروکلریک اسید خاصیته اسیدیته بسیار بالایی دارد و ph آن در دمای اتاق بین 0 تا 2 است.
هیدروکلریک اسید با نام های دیگری مانند هیدروژن کلراید، تیرک، جوهر نمک، اسید کلروهیدریک نیز شناخته میشود. هیدروکلریک اسید خاصیته اسیدیته بسیار بالایی دارد و ph آن در دمای اتاق بین 0 تا 2 است.
این اسید به صورت طبیعی در معده انسان وجود دارد و به هضم غذا کمک میکند. این اسید به دلیل خاصیته اسیدیته بالای خود، کاربرد فراوانی در صنعت دارد ولی این خاصیت آن باعث شده که کار کردن با آن مقداری سخت شود و نیازمند ابزار ایمنی بالایی باشد. ساختار مولکولی هیدروکلریک اسید به صورت زیر است:
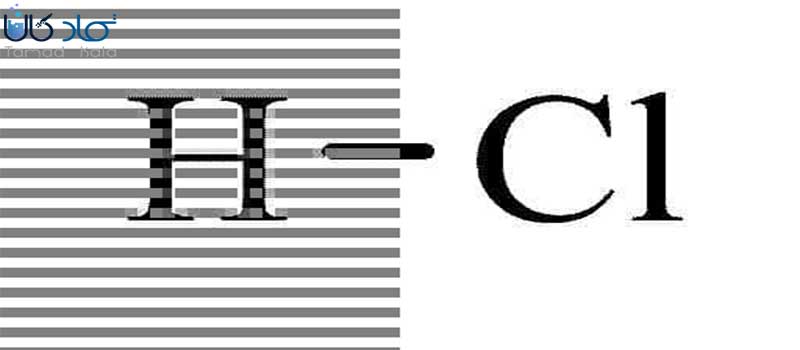
| فرمول شیمیایی | HCl | چگالی | 1.18 g/cm3 |
| جرم مولی | 36.46 g/mol | دمای ذوب | −۲۷٫۳۲ °C (247 K) |
| شکل ظاهری(دمای اتاق) | مایع شفاف | ph | 0 تا 2 |
| دمای جوش | 50/5 °C(for 37% HCl in water) | ویسکوزیته | 1.9 mPa·s at 25 °C 31.5% محلول |
| دمای نگهداری | 2-8 ºC | فشار بخار | 16 kPa(at 20°C) |
ساده ترین روش تولید هیدروکلریک اسید، تزریق گاز هیدروژن کلرید(گاز HCl) به درون آب است. هیدروکلریک اسید کاربرد فراوانی در صنعت دارد به طبع روش های تولید مختلفی در صنعت دارد که هرکدام آن با توجه به کاربرد آن است. یکی از روش های دیگر تولید هیدروکلریک اسید در واحد صنعتی، ترکیب کردن اسید سولفوریک با سدیم کلرید است.
هیدروکلریک اسید با خاصیت اسیدیته بالایی که دارد، در صنعت استفاده های زیاد دارد که در ادامه به برخی از این موارد میپردازیم:
کاربرد هیدروکلریک اسید در تولید مواد شیمیایی
یکی از واکنش های اساسی در صنعت که منجر به تولید مواد شیمیایی میشود، واکنش اسید و باز است. در این واکنش انواع مواد غیر آلی تولید میشود و وابسته به مواد شرکت کننده در واکنش دارند. از دیگر کاربرد های آن، تولید چرم و تولید وینیل کلراید و دی کلرومتان است.
همچنین یکی از واکنش های پر کاربرد هیدروکلریک اسید در صنعت، واکنش آن با آهک است که منجر به تولید کلسیم کلرید میشود که کلسیم کلرید نیز ماده واکنش دهنده بسیار از سایر مواد شیمیایی است و حتی از آن به صورت خالص در برخی صنایع استفاده میکنند.
کاربرد هیدروکلریک اسید در تولید مواد شوینده
هیدروکلریک اسید به دلیل ph کمی که دارد، توانایی جرم گیری و شویندگی بسیار بالایی دارد که البته باید به این مسله توجه کرد که شویندگی آن مربوط به مصارف خونگی نمیشود و بلکه مصارفی که نیاز به ph کمی دارد. برای مثال جرم گیری ابزار و لوله های صنعتی، باز کردن چاه های فاضلاب، یا اسیدیته کردن چاه های نفتی، جرم گیری و تمیز کردن کاشی ها و …
کابرد هیدروکلریک اسید در خنثی سازی
در مواردی که از مواد بازی قوی استفاده شده است و یا حجم ماده ما که ph بالایی دارد، زیاد است؛ برای خنثی کردن آن باید از مقداری زیادی اسید استفاده شود. ساده ترین راه استفاده در حجم کمتر از هیدروکلریک اسید است، زیرا این اسید ph بسیار پایینی دارد و قادر است حجم های بالاتر را که ph تقریبا بالایی دارند خنثی کند.
کابرد هیدروکلریک اسید در رفع زنگ زدگی فولاد
هیدروکلریک اسید رقیق برای رفع و از بین بردن خوردگی مواد فولادی بسیار کاربردی است. حتی برای تولید مواد فولادی و یا دارای فولاد، قبل از استفاده از فولاد آن را به کمک هیدروکلریک اسید تصفیه میکنند و رنگ زدی آن را برطرف میکنند.
کاربرد هیدروکلریک اسید در صنایع نظامی
همانطور که مشخص است، هیدروکلریک اسید کاربرد های فراوانی در صنعت داشته است که کمک بزرگی به ما میکند. اما یکی دیگر از کاربرد های آن تولید بمب شیمیایی است که اولین بار در جنگ جهانی اول اختراع شد و حتی تخمیم زده شد که 80 الی 85 درصد از مرگ و میر های جنگ جهانی اول به خاطر این سلاح مرگبار بوده است.
مونوکسید کربن تصفیه شده با کلر و کاتالیزگر کربن باعث تولید گازی به اسم فسژن میشود. این گاز بی رنگ و با بوی بدی است. استنشاق این گاز باعث هیدرولیز شدن بدن و تخریب دستگاه تنفسی خواهد شد. در نهایت این گاز در بدن به اسید کربنیک و هیدروکلریک اسید تبدیل میشود که اندام های داخلی بدن را از بین میبرد.
کاربرد هیدروکلریک اسید در ساختمان
هیدروکلریک است قادر به تمیزکاری آجر ها است. به این صورت که با کلسیم کربنات واکشن داده و باعث میشود لایه کلسیم کربنات را از روی آجر حذف کند. البته باید به این نکته توجه کنید که این کار نیاز به ایمنی بالایی دارد زیرا این اسید بسیار خورنده است و استنشاق آن باعث بروز مشکلات جبران ناپذیری خواهد شد. واکنش کلسیم کربنات با هیدروکلریک اسید تا جایی که یکی از دو ماده واکنش دهنده ما به اتمام برسد ادامه پیدا خواهد کرد. این واکنش به شرح زیر است:
CaCO3 + 2HCl = CaCl2 + CO2 + H2O
همچنین دیگر کاربرد این ماده، استفاده به عنوان جرمگیر و تمیز کننده قوی در ساختمان سازی است و توانایی لکه بری بالایی دارد. البته که باید توجه شود که سطح مورد استفاده آن از چه جنسی است.

آژانس حفاظت از محیط زیست آمریکا، این ماده را جز مواد خورنده و سمی دانسته است و حفظ ایمنی در هنگام کار با آن را از ضروریات ذکر کرده است. هیدروکلریک اسید خاصیت اسیدیته بسیار بالایی دارد، به خاطر همین باید هنگام کار با آن به موارد زیر توجه شود تا خسارات جبران ناپذیری به وجود نیاید:

در این بخش، به سوالات متداولی که بیشتر درباره هیدروکلریک اسید پرسیده شده است میپردازیم :
آیا هیدروکلریک اسید دارای پیوند هیدروژنی است؟
جواب این سوال خیر است. چرا؟
پیوند هیدروژنی به پیوند بین مولکولی(ثانویه) گفته میشود که در یک مولکول از ماده ما، اتم هیدروژن(H) در کنار یکی از سه اتم اکسیژن(O) یا فلوئور(F) یا نیتروژن(N) باشد، در این صورت، این پیوند به این شکل برقرار میشود که هیدروژن مولکول ما با یکی از سه اتم نام برده شده در مولکول کناری پیوند بین مولکولی هیدروژنی بدهند و همینطور این پیوند های بین مولکولی برقرار میشود. این پیوند الکترونگاتیو بالایی دارد به خاطر همین از پیوند های ثانویه جدا به حساب میاید.
تفاوت هیدروژن کلرید با هیدروکلریک اسید چیست؟
هیدروکلریک اسید همانطور که گفته شد یک اسید بسیار قوی با فرمول شیمیای HCl است ولی هیدروژن کلرید یک گاز با ترکیب شیمیایی HCl است. پس تنها تفاوت این دو، حالت فیزیکی آن ها است. البته به این موضوع نیز باید دقت شود که در برخی مواقع (اکثرا در صنعت) این دو مورد را یکی میدانند ولی طبق نامگذاری آیوپاک این دو متفاوت هستند.
تفاوت هیدروکلریک اسید با جوهر نمک چیست؟
هیچ تفاوتی ندارد و جوهر نمک نام دیگر هیدروکلریک اسید است که معمولا در صنعت از این اسم استفاده میشود.
هیدروکلریک اسید را از کجا تهیه کنیم؟
فروشگاه تمادکالا مفتخر است با ارائه انواع مواد شیمیایی آزمایشگاهی و صنعتی با کیفیت تضمین شده و قیمت مناسب، رضایت مشتریان عزیز را جلب کند. فروش هیدروکلریک اسید در مقادیر دلخواه و برند های متفاوت به صورت آنلاین در کمترین زمان در فروشگاه تمادکالا صورت می پذیرد.
شما می توانید برای خرید هیدروکلریک اسید به صورت آنلاین از طریق لینک پیوست شده در زیر اقدام فرمایید. فروشگاه تمادکالا جهت رفاه حال مشتریان، امکان ارسال محصولات خود را به اقصی نقاط ایران فراهم کرده است.
واکنش آهن و یا فلزات با هیدروکلریک اسید به چه صورت است؟
هیدروکلریک اسید یک اسید قوی است و واکنش اسید با فلزات یک واکنش معروف در صنعت است. هیدروکلریک اسید رقیق شد با آهن واکنش میدهد و گاز هیدروژن آزاد میکند که معادله شیمیایی آن در زیر آمده است:
Fe+2HCl→FeCl2+H2
دلیل متفاوت بودن نقطه جوش محلول هیدروکلریک اسید چیست؟
همانطور که گفته شد، هیدروکلریک اسید خاصیت اسیدیته بالایی دارد به خاطر همین در هیچ یکی از مصارف آن از آن به طور 100 درصد خالص استفاده نمیکنند. بسته به اینکه چه کاربردی دارد، درصد آن متفاوت است و این متفاوت بودن آن و مخلوط شدن آن با آب باعث تفاوت در نقطه جوش خواهد شد. هرچه درصد آن کمتر باشد، نقطه جوش بالایی دارد زیرا آب به دلیل داشتن پیوند هیدروژنی، نقطه جوش بالاتری نسبت به هیدروکلریک اسید دارد.
ضدعفونی کردن دستان روشی مطمئن و مقرون به صرفه برای پیشگیری از بیماری های واگیر دار به ویژه ویروس کرونا است. طبق تحقیقات انجام شده ضدعفونی کردن دستان باعث کاهش 50% مرگ و میر ناشی از اسهال و کاهش 25% مرگ و میر ناشی از عفونت های تنفسی می شود. ضدعفونی کننده های دست اولین […]
اسید سولفوریک یا جوهر گوگرد، یک اسید معدنی بسیار قوی با فرمول شیمیایی H2SO4 و چگالی 1.83 g/cm3 است. اسید سولفوریک برای اولین بار با تقطیر زاج سبز با مس(II) سولفات توسط جابر ابن حیان تولید شد. اسید ساختار قطبی دارد و با هر نسبتی در آب حل میشود. این اسید به دلیل داشتن پیوند […]
ذغال فعال یا کربن فعال(Activated Carbon) یکی از موادی است که امروزه در داروخانه و زیبایی کاربرد بسیار زیادی پیدا کرده است. در مقاله پیشرو به معرفی کربن فعال و کاربردهای آن در زیبایی خواهیم پرداخت. کربن فعال نوعی کربن است که دارای منافذ بسیار زیادی است. این ماده بدلیل منافذ فراوان و تخلخل بسیار […]
روش کشت باکتری در محیط جامد محیط کشت جامد به دو صورت وجود دارد: محیط کشت جامد در لوله محیط کشت جامد در پلیت در لوله به دوصورت عمودی (Stab Culture) و شیبدار (Slant Culture) دیده می شود که هر کدام از آنها روش کشت خاص خود را دارند. روش کشت عمقی در لوله : […]
متشکرم