هیدروکسید سدیم (NaOH) یک جامد قلیایی سفید رنگ و بی بو است. معمولاً به عنوان سود سوزآور شناخته میشود. این یک ترکیب معدنی بسیار سوزاننده و واکنش پذیر است. این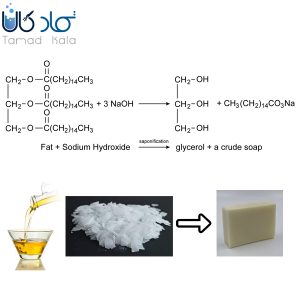 موضوع باعث میشود که بسیاری بپرسند آیا استفاده از هیدروکسید سدیم در صابون و لوازم آرایشی بی خطر است؟ پاسخ کوتاه این است که بله، زیرا با وجودی که از هیدروکسید سدیم در صابونسازی استفاده میشود، اما در قالب واکنش صابونی شدن، دیگر خواص سودسوز آور را ندارد و همچنین در بسیاری از فرایندهای شیمیایی تولید محصولات مختلف، از جمله لوازم آرایشی و بهداشتی، از هیدروکسید سدیم در غلظتهای پایین به عنوان تثبیت کننده pH یا تنظیم کننده pH استفاده میشود. هیدروکسید سدیم همچنین در بسیاری از محصولات خانگی رایج دیگر از جمله پاک کنندههای فاضلاب، داروها و در برخی از محصولات غذایی استفاده میشود.
موضوع باعث میشود که بسیاری بپرسند آیا استفاده از هیدروکسید سدیم در صابون و لوازم آرایشی بی خطر است؟ پاسخ کوتاه این است که بله، زیرا با وجودی که از هیدروکسید سدیم در صابونسازی استفاده میشود، اما در قالب واکنش صابونی شدن، دیگر خواص سودسوز آور را ندارد و همچنین در بسیاری از فرایندهای شیمیایی تولید محصولات مختلف، از جمله لوازم آرایشی و بهداشتی، از هیدروکسید سدیم در غلظتهای پایین به عنوان تثبیت کننده pH یا تنظیم کننده pH استفاده میشود. هیدروکسید سدیم همچنین در بسیاری از محصولات خانگی رایج دیگر از جمله پاک کنندههای فاضلاب، داروها و در برخی از محصولات غذایی استفاده میشود.
کاربردهای زیادی از هیدروکسید سدیم وجود دارد. هیدروکسید سدیم یک ترکیب همه کاره است که برای تولید انواع محصولات حتی کاغذ و فرآوردههای نفتی هم استفاده میشود. همچنین در بسیاری از محصولات خانگی یافت میشود که برخی از آنها عبارتند از:

اگر می خواهید اطلاعات کاملی در خصوص سدیم هیدروکسید کسب کنید به بخش کاربرد سدیم هیدروکسید مراجعه کنید.
پوست بدن انسان، pH اش به سمت pHهای اسیدی است و معمولاً بین 4 تا 7 متغیر است. حفظ این اسیدیته (معروف به “جبه اسیدی”) لایه ای از محافظت (فلور نرمال) در برابر عوامل محیطی مانند آلرژنها، آلایندهها و باکتریها را فراهم میکند. اگر pH محصولات مراقبت پوستی، از pH طبیعی پوست، فاصله داشته باشد، محافظت اسیدی پوست دچار اختلال میشود، که ممکن است خطر پیری زودرس را نیز افزایش دهد. استفاده از محصولات مراقبتی پوست با غلظتهای کم هیدروکسید سدیم، بسیار ایمنتر است.
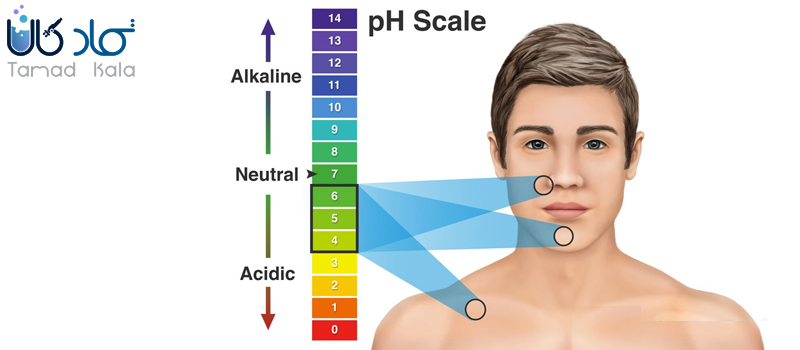
بنابراین استفاده از سدیم هیدرکسید در محصولات آرایشی و بهداشتی معمولا فقط برای تنظیم pH در بازه مطلوب برای پوست، مناسب است نه اینکه محصولاتی با pH بالاتر از pH پوست تولید شود.
صابون از نظر فنی یک محصول نمکی است که از ترکیب یک قلیا با چربی یا اسیدهای چرب ساخته میشود. ترکیب قلیایی، همان ترکیب بازی است که بعد از تولید صابون، مسئول ایجاد حالت لیز است. چربیها (یا اسیدهای چرب) همان روغنها هستند.
هیدروکسید سدیم یک مادهای است که در یک واکنش شیمیایی برای تولید مواد دیگر استفاده میشود. سود سوزآور یک عنصر ضروری در صابون سازی است و باعث انجام شدن فرایند صابونی شدن میشود. وقتی تکهها یا دانههای هیدروکسید سدیم به مایع اضافه شوند، محلول سدیم هیدروکسید تشکیل میشود؛ محلول سدیم هیدروکسید شامل یونهای تفکیک شدهی سدیم و هیدروکسید است. این محلول در صورت مخلوط شدن با روغن یا چربی منجر به واکنش شیمیایی به نام «صابونی شدن» میشود.
امروزه بیشتر صابون سازیهای صنعتی از طریق یک فرآیند مداوم انجام میشود که به جای دستههای کوچک، جریان ثابتی از صابون تولید میکند. تولیدکنندگان ابتدا چربیهای طبیعی را به اسیدهای چرب و گلیسیرین تقسیم میکنند، معمولاً از طریق یک ستون فولادی بلند و عمودی به نام هیدرولیز که از دمای بالا برای شکستن چربی به دو جزء آن استفاده میکند. پس از جدا شدن، اسیدهای چرب برای خالص سازی بیشتر تقطیر میشوند. سپس، اسیدهای چرب خالص شده با مقدار دقیق اندازه گیری شده از سود سوزآور، مخلوط میشوند. با ادامه فرایند، صابون ایجاد میشود. در طول این مرحله، ممکن است مواد شیمیایی دیگری برای افزایش ماندگاری، قدرت پاککنندگی یا بازارپسندی اضافه شود مثل اسانسهای طبیعی مثل اسانس روغنی اسطوخدوس، اسانس رز و … که علاوه بر بازار پسندی، میتوانند خاصیت درمانی یا زیبایی هم داشته باشند. اما میتوانید صابون مایع را با سود سوزآور در دستههای کوچک نیز تهیه کنید. شما میتوانید دستور العملهای مختلفی برای تهیه صابون مایع دسته کوچک پیدا کنید، اما روند کلی واکنش شیمیایی صابونی شدن، یکسان است.
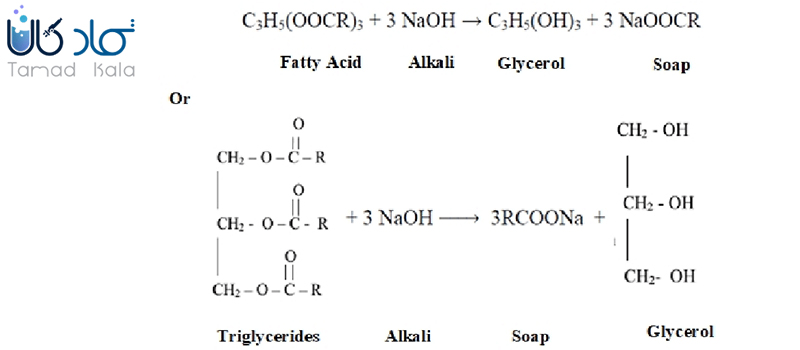
در ابتدایی ترین سطح خود، ساخت صابون برای شروع فرآیند شیمیایی صابون سازی به هیدروکسید سدیم، آب و روغن/چربی نیاز است. آب و چربی به خودی خود خوب با هم مخلوط نمیشوند. در اینجا نقش سدیم هیدروکسید نمایان میگردد. هنگامی که سدیم هیدروکسید به آب اضافه می شود (نه برعکس!)، یک واکنش گرمازا ایجاد میکند، به این معنی که خیلی سریع گرم میشود. سپس صابون سازها این محلول آبی سدیم هیدروکسید را با پایه روغن یا چربی ترکیب میکنند تا صابون تولید کنند.
سدیم هیدروکسید با روغن مخلوط میشود و صابون تولید میشود. در ابتدا، سدیم هیدروکسید، آب و روغن دارید. سپس فرآیند پخت (cure) آغاز میشود و پس از چند روز، سدیم هیدروکسید، آب و روغن به صابون تبدیل میشود. در پایان فرآیند پخت، شاید 3 تا 4 هفته (گاهی اوقات بیشتر)، نه سدیم هیدروکسید در صابون باقی میماند، نه روغن و نه آب، بلکه چیزی که باقی میماند صابون خالص است. بنابراین به طور خلاصه، هیدروکسید سدیم میتواند روغنها را تبدیل به صابون کند. و این بدان معناست که به روغنها و چربیها کمک میکند تا کف کنند و خاصیت صابونی داشته باشند.
ایمنی هیدروکسید سدیم به شدت به سطح غلظت بستگی دارد، با غلظتهای بالاتر مشکلات ایمنی (یا safety) بیشتری را ایجاد میکند. عوامل دیگری که بر ایمنی تأثیر میگذارند عبارتند از: مدت زمان قرار گرفتن در معرض، منطقه در معرض و شرایط محیطی. هیدروکسید سدیم بسیار سوزاننده و خورنده است و در صورت استنشاق ممکن است باعث تحریک پوست و چشم یا مشکلات تنفسی شود. هرگز نباید هیدروکسید سدیم خالص را روی پوست بریزد. سدیم هیدروکسید میتواند علائم پوستی مانند سوختگیهای شیمیایی خفیف تا شدید یا سوراخهایی در پوست و بافتهای زیرین ایجاد کند.

هیدروکسید سدیم در بسیاری از لوازم آرایشی با غلظت کم (اغلب 5% یا کمتر) وجود دارد. با توجه به بررسی کارگروههای محیط زیست ایالات متحده (EWG)، وجود هیدروکسید سدیم در محصولات مراقبت شخصی، با سرطان، مسمومیت، رشد و تولید مثل، و همچنین آلرژی یا سمیت ایمنی مرتبط نیست. سازمان غذا و داروی ایالات متحده (FDA)، هیدروکسید سدیم را برای استفاده به عنوان یک افزودنی غذایی در سطوح کمتر از 1% درصد، ایمن تأیید کرده است.
فیلتر های سرسرنگی دسته ای از فیلتر ها هستند که برای فیلتر کردن مایعات با حجم پایین بسیار مناسب هستند. در مقاله پیش رو شما را با این فیلتر ها بیشتر آشنا می کنیم. فیلتر سر سرنگی چیست؟ فیلتر های سرسرنگی به فیلتر هایی گفته می شود که در سر سرنگ ها متصل می شوند […]
کود چیست؟ به هرنوع ماده آلی، معدنی یا بیولوژیکی که دارای عناصر غذایی باشد و باعث بالابردن حاصلخیزی خاک یا افزایش عملکرد کیفی و کمی محصول شود، کود گفته میشود. کودها به طور کلی به سه دسته تقسیم میشوند: کودهای شیمیایی کودهای آلی یا ارگانیک کودهای بیولوژیک یا زیستی کودهای شیمیایی یکی از انواع مهم […]
دانلود فایل PDF مقاله دستگاه DSC برای اندازه گیری اختلاف جریان گرما بین نمونه و مرجع طراحی شده است. دو نوع دستگاه متداول کالری سنجی روبشی افتراقی وجود دارد: کالری سنجی روبشی افتراقی مبتنی بر اندازه گیری شار حرارتی(Heat flux DSC) و کالری سنجی روبشی افتراقی مبتنی بر اندازه گیری توان الکتریکی(Power-compensated DSC). درخواست آنالیز […]
طول یکی از کمیت هایی است که واحد های مختلفی دارد و تعداد زیادی از این واحد ها امروزه در نقاط مختلف جهان استفاده میشوند. مشکلی که در حال حاضر وجود دارد، این است که کشورهای مختلف واحدهای طولی متفاوتی را به رسمیت میشناسند. این تفاوت واحدهای طول در کشورهای مختلف، مشکلات زیادی را فراهم […]