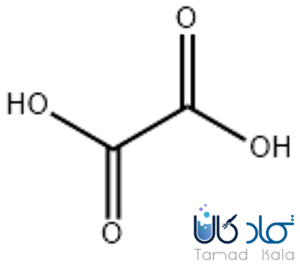
برای اولین بار، اگزالیک اسید در سال 1776 تولید شد. اسید اگزالیک یک اسید آلی دو ظرفیتی است که به صورت نمکهای پتاسیمی و کلسیمی در گیاهان و سبزیجات یافت میشود. غلظت اگزالیک اسید در گیاهان و سبزیجات معمولا کم است. به علاوه اگزالیک اسید در بدن از طریق متابولیسم گلایوکسیلیک اسید یا اسکوربیک اسید تولید میشود. به طور کلی، اگزالیک اسید در بدن متابولیسم نمیشود، و از طریق ادرار از بدن دفع میشود. همانطور که در ساختار اگرالیک اسید دیده میشود، این اسید در واقع از اتصال دو گروه کروکسیل اسید ایجاد میشود و به همین علت، اگزالیک اسید یک اسید آلی قوی به حساب میآید.
اگزالیک اسید در گیاهانی مثل برگ گندم سیاه، فلفل سیاه، خرفه، ریواس، برگ چای، کاکائو، کاهوی تلخ، اسفناج، زنجبیل، موز، بادام هندی، بادام، ریشه سیب زمینی شیرین، کدو تنبل، جوی دو سر، و برگهای مختلف کلم، یافت میشود. بنابراین اگزالیک اسید به عنوان یک مادهای که در انواع پسماندهای آلی گیاهی کمپوست شده وجود دارد.
اگزالیک اسید علاوه بر ویژگیهای معمول که همه کربوکسیلیک اسیدها دارند، کاهنده قوی است به طوری که میتواند منگنز هفت ظرفیتی را در ترکیب پتاسیم پرمنگنات را طی واکنش زیر به منگنز دو ظرفیتی در ترکیب منگنز سولفات تبدیل کند:
5 C2H2O4 + 2 KMnO4 + 3 H2SO4 → K2SO4 + 2 MnSO4 + 8H2O + 10 CO2
اگزالیک اسید قابلیت واکنش با اکثر فلزات را دارد و میتواند نمکهای اگزالات مختلفی را تولید کند. البته به جز نمکهای فلزات قلیایی و نمکهای فلزات دو ظرفیتی، سایر نمکهای اگزالات به طور جرئی در آب حل میشوند و قابلیت تشکیل کمپلکس در آب را دارند. همچنین اگزالات و نمکهای اگزالیک اسید سمیت دارند. اگزالات جزء شیمیایی با ساختار شیمیایی زیر است:
اگزالیک اسید به خاطر داشتن گروههای عاملی آبدوست، ترکیبی آبدوست است که در آب حل میشود و میزان حلالیت آن در آب 108 گرم در 1 لیتر آب در دمای 25 درجه سانتی گراد است. همچنین با انحلال 100 گرم اگزالیک اسید در 1 لیتر آب در دمای 20 درجه سانتی گراد، pH محلول برابر با 1 خواهد بود. اگزالیک اسید علاوه بر آب، قابلیت انحلال در اتانول و اتر را دارد.
برای تهیه اگزالیک اسید، ابتدا سدیم فرمات به همراه سدیم هیدروکسید حرارت میدهند تا سدیم اگزالات تشکیل شود و به کلسیم اگزالات تبدیل شود و سپس در معرض سولفوریک اسید قرار بگیرد تا اگزالیک اسید به دست بیاید.
همچنین برای تولید اگزالیک اسید، از واکنش نیتریک اسید با شکر، نشاسته و یا سلولز هم میتوان استفاده کرد.
اگزالیک اسید به عنوان یک جزء شیمیایی در کاربردهای شیمی تجزیه استفاده میشود.
در مقایسه با سایر کربوکسیلیک اسیدها (به جز فرمیک اسید)، اگزالیک اسید به سادگی اکسید میشود و به همین دلیل یک عامل کاهنده قوی به حساب میآید و به خاطر همین ویژگی، در کاربردهای عکاسی، سفید کنندگی (bleaching) و پاک کردن جوهر استفاده میشود.
از اگزالیک اسید برای تولید بسیاری از ترکیبات اگزالات مثل اگزالات استر آمید، استفاده میشود.
از این ماده به طور گسترده در تولید داروهایی مثل آنتی بیوتیکها استفاده میشود.
اگزالیک اسید به عنوان یک حلال خوب برای استخراج فلزات نادر به کار میرود.
اگزالیک اسید برای برخی از واکنشها به عنوان کاتالیست عمل میکند، مثلا واکنش تولید کبالت-مولیبدن-آلومینا.
همچنین برای پاک کردن سطح فلزات هم استفاده میشود.
اگزالیک اسید را معمولا در بطریهای شیشهای نگهداری میکنند تا از آسیبهای احتمالی جلوگیری شود. سپس آن را در محلی خشک و خنک که تهویه هوا داشته باشد، نگه میدارند. همچنین بهتر است در جایی باشد که احتمال اشعال پذیری کمتری داشته باشد و به دور از مواد شیمیایی آنتی اکسیدان باشد.
گلیسیرین چیست؟ گلیسیرین که با نامهای (1,2,3-Trihydroxypropane، Glycerin ،Glycerol) نیز شناخته می شود، یک الکل قندی تری هیدروکسی است که دارای متابولیسم کربوهیدرات و لیپید است. دارای فرمول مولکولی ( C3H8O3 یا CH2OH-CHOH-CH2OH ) و جرم مولکولی 92.094 g/mol است. همچنین به دلیل داشتن پیوند هیدروژنی ( 3 گروه هیدروکسیل) با هر نسبتی با آب […]
استفاده از کود ها در صنعت کشاورزی امروزه بسیار مورد توجه بوده است درختان برای بار دهی مناسب و عالی علاوه بر خاک مناسب و نور و شرایط آب و هوا نیاز به استفاده از کود نیز دارند. یکی از مناسب ترین کود های تقویت خاک درختان و گیاهان کود گوگرد گرانوله است که این […]
اسید نیتریک یک ترکیب شیمیایی با فرمول HNO3 و جرم مولکولی 63.01g/mol است. اسید نیتریک قابلیتی اسیدیته بسیار بالایی دارد و برای همین از قابلیت انحلال آن در صنعت استفاده فراوانی میشود. نام های دیگر اسید نیتریک، جوهر شوره و تیزاب است. اسید نیتریک خالص مایعی بی رنگ حساس به نور است که به مرور […]
شناساگر ماده ای است که با تغییر شرایط محلول دچار تغییر قابل مشاهده ی مشخصی می شود. این تغییر می تواند تغییر رنگ، تشکیل رسوب، تشکیل حباب، تغییر دما یا کیفیت قابل اندازه گیری دیگری باشد. یکی از روش های شناسایی واکنش های شیمیایی و واکنش های فیزیکی، استفاده از شناساگرها است. نوع دیگری از […]