- فروش مواد شیمیایی
- مواد اولیه صنایع غذایی
- فروش ظروف آزمایشگاهی
- فروش تجهیزات
- مطالب مفید
- آگهی رایگان
- پیشنهادهای ویژه
- آموزش کار با سایت
- ورود به حساب کاربری
کلمه آمینو اسید کوتاه شده عبارت آلفا-آمینو کربوکسیلیک اسید است. آمینو اسیدها مولکولهایی آلی هستند که از یک گروه آمینو (-NH2)، کربوکسیل (-COOH) و یک زنجیره آلی R ساخته شده اند. ترکیب این زنجیره آلی در هر یک از آمینواسیدها کاملا یکتاست. هر مولکول شامل یک کربن مرکزی است که آلفا-کربن نامیده می شود و گروه های کربوکسیل و آمینو به آن متصل اند. دو پیوند دیگر کربن که آزاد مانده است، با هیدروژن و زنجیره R پیوند می دهد. آمینواسیدها با توجه به ترکیب شیمیایی خاص گروه R از یکدیگر متمایز می شوند. فرمول کلی آمینواسیدها به صورت زیر نمایش داده می شود.
اسیدهای آمینه واحدهای سازنده پروتئین هستند. در حدود 20 درصد بدن انسان را پروتئین ها تشکیل دادند که تقریبا در تمامی فرآیندهای بیولوژیکی بدن نقش دارند. به عبارتی دیگر، آمینواسیدها نقش کلیدی در بدن ایفا می کنند و از اهمیت بالایی برخوردارند. آمینواسیدها در سلول ها، عضلات، پوست، استخوان و بافت های بدن وجود دارد و بخش زیادی از آن ها را شامل می شود. آمینواسیدها بر اساس اینکه در بدن به طور طبیعی بتوانند تولید شوند یا نه در دو گروه آمینو اسیدهای ضروری و غیر ضروری قرار می گیرند. آمینواسیدهای ضروری، آمینو اسیدهایی هستند که برای رفع نیاز بدن باید از طریق مصرف منابع غذایی متعدد به مقدار لازم به بدن برسند. این گروه از آمینو اسیدها در مواد غذایی لبنی و گوشت و تخم مرغ و غلات یافت می شوند. گروه دیگر که آمینواسیدهای غیر ضروری نام دارند، بدن توانایی تولید آن ها را داشته و تنها در صورت بیماری این نوع آمینواسید تولید نمی شود. آمینواسیدهای ایزولوسین، لوسین، لیزین، متیونین، فنیل آلانین، ترئونین، تریپتوفان و والین، 8 آمینواسید ضروری بدن هستند.
تمادکالا این امکان را فراهم کرده است که به راحتی انواع آمینواسید ها را خریداری کنید . کافی است با مراجعه به صفحه زیر لیست انواع اسید آمینه را در تمادکالا مشاهده کنید.
آمینواسیدهای استاندارد بر حسب قطبیت و بار گروه R به چهار گروه اصلی تقسیم می شوند.
گروه اول آمینواسیدهای ناقطبی: این گروه از آمینو اسیدها به دلیل عدم وجود گروه های باردار و یا قطبی در گروه R، باعث آبگریز شدن آمینواسید می شود. آلانین، گلیسین، والین، لوسین و ایزولوسین، آمینواسیدهای آبگریزی هستند که دارای گروه متیل هستند و میزان آبگریزی از آلانین به ایزولوسین به دلیل افزایش تعداد گروه های متیل افزایش می یابد.
گروه دوم آمینواسیدهای قطبی بدون بار: آمینواسیدهای سرین، سیستئین، ترئونین، تیروزین، آسپارژین و گلوتامین در این گروه قرار می گیرند. وجود گروه عاملی الکل در مولکول سرین و ترئونین باعث ایجاد پیوند هیدروژنی با مولکول های آب شده و به راحتی در آب حل می شوند. به زنجیره حلقوی در تیروزین، عامل هیدروکسیل متصل است که قطبیت آن را افزایش می دهد.
گروه سوم آمینواسیدهای قطبی با بار منفی: گلوتامیک اسید و آسپارتیک اسید در این گروه جای دارند. حضور عامل کربوکسیل در زنجیره کناری این نوع آمینواسیدها باعث قطبیت این مولکول شده و به راحتی با از دست دادن H+، کربوکسیل با بار منفی ایجاد می شود.
گروه چهارم آمینواسیدهای قطبی با بار مثبت: زنجیره کناری آمینواسیدهای لیزین، آرژنین و هیستیدین دارای گروه آمین هستند که در pH خنثی بار مثبت دارند. لیزین یک عامل آمین، آرژنین یک عامل گوآنیدیوم و هیستیدین یک گروه ایمیدازول دارد. حضور این گروه ها باعث افزایش بار مثبت در زنجیره پروتئینی شده و مولکول خاصیت قلیایی از خود نشان خواهد داد.
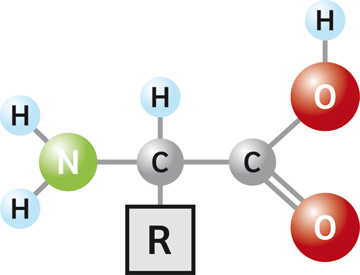
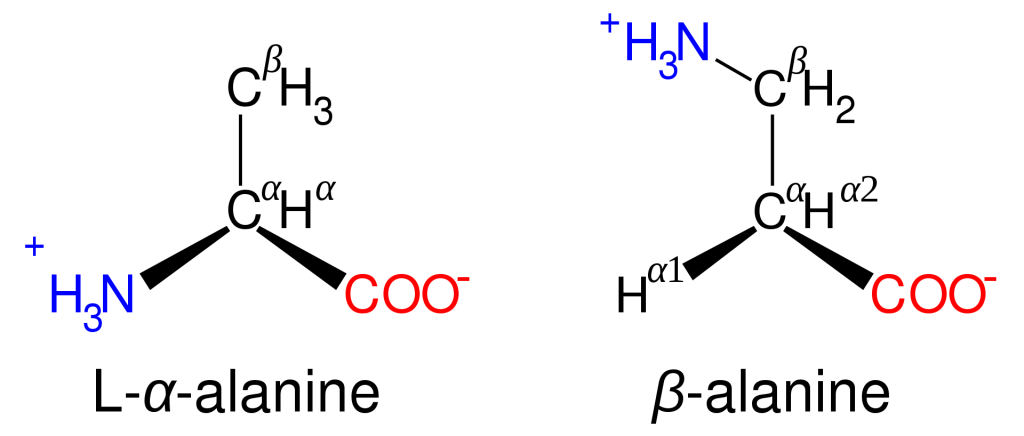
در تصویر بالا می توانید ساختار کلی یک آمینواسید را مشاهده فرمایید. گروه R که در تصویر قابل مشاهده است، نشان دهنده یک گروه جانبی مشخص است که در هر آمینو اسید این گروه متفاوت است. کربنی که در کنار گروه کربوکسیل(COOH) است، با نام کربن آلقا شناخته می شود. آمینواسیدهایی که در آنها گروه آمینی مستقیما به کربن آلفا متصل باشد، آلفا آمینواسیدها نامید می شوند. در آمینواسیدهای آلفا، هر دو گروه هیدروکسیل (COOH) و آمینی(NH2) به یک کربن (که با نام کربن آلفا شناخته می شود) متصل هستند. در تصویر زیر یک مثال از آمینو اسید آلفا و تفاوت آن با آمینو اسید بتا آمده است:
عمده آلفا آمینواسیدهایی که در طبیعت یافته می شوند، از نوع L هستند. تقریبا تمامی آلفا آمینواسیدها می توانند دو جهتگیری فضایی قرینه یکدیگر داشته باشند که با نام های L و D شناخته می شوند. این دو انانتیومر در خرید آمینواسیدها نیز اهمیت زیادی دارند و باید به آنها توجه شود.(برای اطلاعات بیشتر، لازم است که درباره کایرالیته مطالعه فرمایید.) در تصویر زیر میتوانید تفاوت آمینواسیدهای نوع L و D را مشاهده فرمایید. (در این تصویر توجه فرمایید که اگر دست چرخانده شود، به همان شکل نخواهیم رسید و پشت و روی دست با یکدیگر متفاوت هستند. به همین دلیل نیز اگر آمینو اسید نوع L را بچرخانیم، نمی توانیم توقع داشته باشیم که آمینواسید نوع D بدست آمده باشد و همچنان همان آمینواسید نوع L است. برای درک بهتر این موضوع، لازم است تا آمینواسیدها را به صورت ساختار فضایی 3 بعدی تصور کنید.)
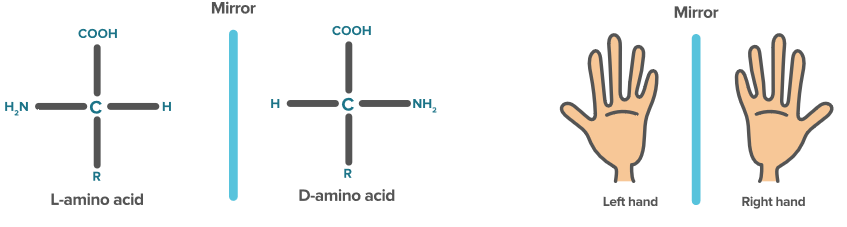
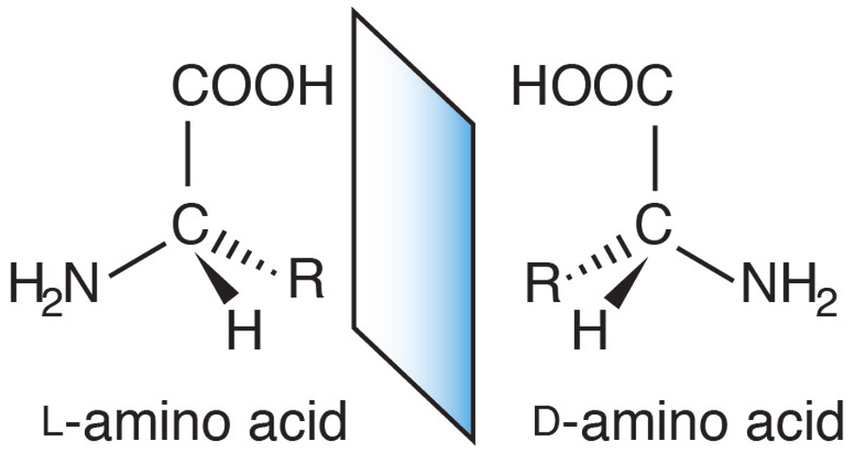
همانطور که گفته شد، عمدتا آمینواسیدهای موجود در طبیعت و بدن، آمینواسیدهای نوع L هستند.
در تصویر بعدی، یک اینفوگرافیک است که آمینواسیدهای مختلف را نمایش می دهد:
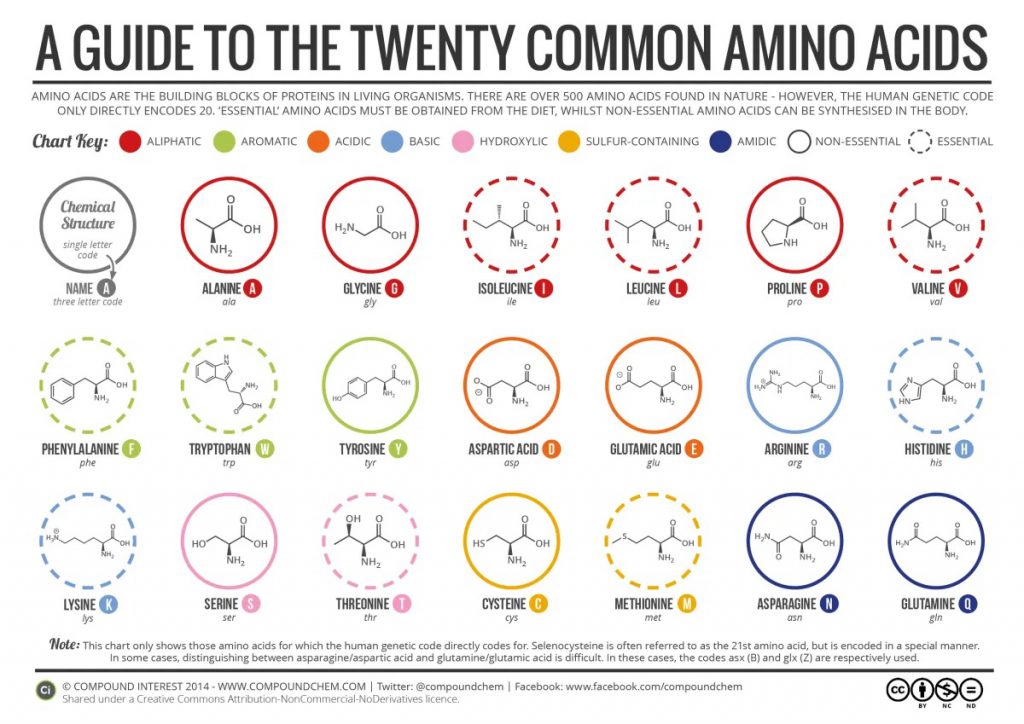
با اتصال آمینواسید ها به یکدیگر، پروتئین ها ساخته می شوند. این پیوند که بین آمینواسیدها وجود دارد، پیوند پپتیدی نامیده می شود؛ به همین دلیل نیز هست که به پروتئین ها پلی پپتید نیز گفته می شود. به طور کلی پروتئین ها نسبت به شرایط محیطی مختلف حساس هستند و با تغییرات دما و pH، ممکن است تغییر شکل داده(denature شوند) و کارکرد خود را از دست بدهند. به همین دلیل هم هست که ما نمیتوانیم پروتئین ها را به صورت مستقیم جذب کنیم. وقتی می گوییم یک ماه غذایی دارای پروتئین است و باعث جذب پروتئین می شود، منظورمان این است که آمینواسیدهای آن جذب می شوند. آمینواسیدها در داخل بدن، استفاده شده و تبدیل به پروتئین ها می شوند.
آمینواسیدها در داخل سلول، توسط اندامکی با نام ریبوزوم، استفاده شده و برای ساخت پروتئین ها استفاده می شوند. ژن های سلول ترجمه شده و بر اساس ژن ها، ریبوزوم پروتئین های مختلف را تولید می کند. حتی زمانی که پروتئینی کارکرد خود را از دست بدهد، مجددا تبدیل به آمینواسید شده و در این اندامک برای ساخت پروتئین ها استفاده خواهد شد.
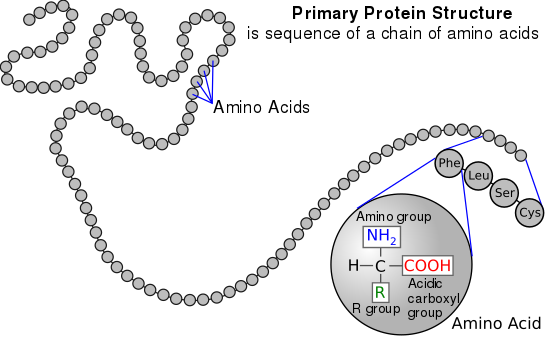
آمینواسیدها به تنهایی و یا در ترکیب با یکدیگر به عنوان تقویت کننده طعم ماده غذایی به کار می رود. گلیسین و آلانین دو آمینو اسیدی هستند که باعث تقویت طعم و مزه می شوند. تریپتوفان و هیستیدین در ترکیب با یکدیگر، می توانند به عنوان یک آنتی اکسیدان برای حفظ پودر شیر عمل کنند. سیستئین نیز آنتی اکسیدانی است که برای حفاظت از آبمیوه ها مناسب است. برخی آمینواسیدها مانند لیزین، متیونین، ترئونین و تریپتوفان در پروتئین های گیاهی به صورت کم و محدود وجود دارد. افزودن این آمینواسیدها به ماده غذایی باعث بهبود ارزش غذایی و طعم آن می شود.
آمینواسیدها می توانند به عنوان دارو مصرف شوند. به طور مثال آمینواسیدهای ضروری برای درمان بیماران پس از عمل به کار می روند.
آمینواسیدها مواد اولیه برای تولید ترکیبات مختلفی به شمار می روند. گلیسین به عنوان پیش ماده برای سنتز گلیفوسات و ترئونین برای ساخت ازترئونام، استفاده می شود. همچنین برای تهیه چرم از پلی متیل گلوتامات استفاده می شود. برای ساخت مواد آرایشی و بهداشتی نیز به آمینو اسید نیاز است.
امیدوارم این سری از مقالات تمادکالا برای شما مفید واقع شده باشد. شما می توانید سوالات خود را در ادامه این مقاله مطرح کنید.
قیف های آزمایشگاهی انواع مختلفی دارند و در آزمایشگاه ها بسیار استفاده میشوند. بیشتر کاربرد آنها برای جمع کردن ماده ای خاص درون ظرفی دیگر است. در مقاله پیش رو قصد داریم به بررسی انواع و کاربردهای این قیف ها بپردازیم. قیف آزمایشگاهی عموما برای استفاده در آزمایشگاه های شیمی ساخته شده است. البته درحال […]
برای ضد عفونی کردن دست ممکن است از مواد مختلفی استفاده شود. اما پرکاربردترین آنها الکل ها هستند. در مقاله پیش رو قصد داریم توضیحات بیشتری در این باره ارائه کنیم. عمده ضدعفونی کننده های دست که در بازار یافت می شوند، بر پایه الکل هستند. الکل ها قابلیت تخریب پروتئین های ویروس، باکتری یا […]
کات کبود یا مس(||)سولفات که فرمول شیمیایی آن CuSO45 آبه میباشد نمکی آبی رنگ است که به صورت گرماده در آب حل میشود. سولفات مس یا زاج کبود ترکیبی غیرآلی است که در حیطههای مختلفی از جمله صنعت، آموزش، کشاورزی و حتی پزشکی به کار میرود. سولفات مس دارای خاصیتی سمی است که میزان سمیت […]
بالن یا فلاسک آزمایشگاهی یکی از لوازم بسیار پرکاربرد در آزمایشگاه هاست که در هر آزمایشگاهی لازم و ضروری است. شناخت انواع بالن آزمایشگاهی و دانستن کاربرد هرکدام، به استفاده بهتر در آزمایشگاه و انتخاب بالن مناسب، کمک خواهد کرد. در این مقاله با انواع بالن آزمایشگاهی و کاربرد هریک آشنا می شویم. بالن آزمایشگاهی […]